Le glaucome à pression normale
Un OVNI dans le monde du glaucome
Son mécanisme est discuté
Par définition, le glaucome à pression normale (GPN) est caractérisé par une neuropathie optique évolutive identique à celle du glaucome chronique à angle ouvert, mais avec une tension oculaire constamment inférieure ou égale à 21 mm de mercure pendant six semaines consécutives et sans aucun traitement. Les études épidémiologiques montrent que 30 % des glaucomes primitifs à angle ouvert sont des glaucomes à pression normale en Occident, alors qu’en Extrême-Orient ces glaucomes représentent 80 % des glaucomes. Cette pathologie est plus fréquente chez la femme, elle est génétiquement déterminée. Certains gènes ont été identifiés (OPTN, OPA1 et APOE). La prévalence augmente avec l’âge : dans la Beaver Dam Eye Study, la prévalence est de 0,2 % entre 40 et 54 ans et elle monte à 1,6 % au-delà de 75 ans. Sur le plan physiopathologique, depuis de nombreuses années, deux théories s’affrontent : la théorie vasculaire et la théorie mécanique, mais parmi cette dernière plusieurs processus en cause permettent d’expliquer la multiplicité des tableaux cliniques.
La théorie vasculaire
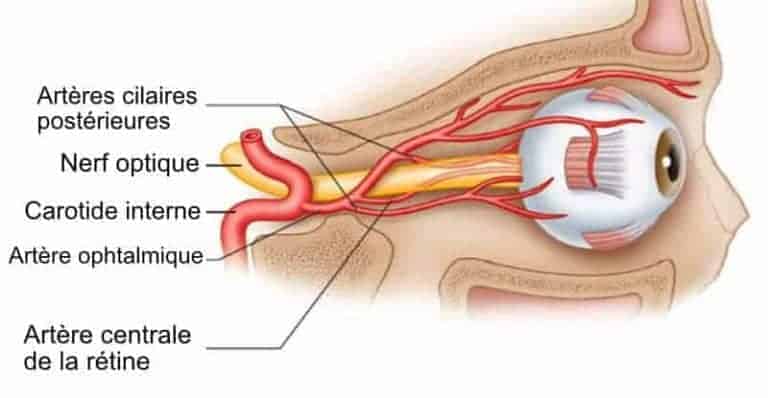
La vascularisation de type terminal de la tête du nerf optique, dépendant à 100% de la carotide interne par l’intermédiaire de l’artère ophtalmique, a pu faire évoquer une particulière fragilité de ce réseau vasculaire qui souffre rapidement en cas d’anomalies vasculaires plus générales. L’artère centrale de la rétine et les artères ciliaires sont toutes des branches de l’artère ophtalmique issue de la carotide interne. Toute atteinte du réseau de l’artère ophtalmique ne pourra être suppléée par d’autres branches artérielles.
Arguments en faveur de la théorie vasculaire
- l’hypotension artérielle, encore plus l’hypotension artérielle diastolique et nocturne sont des facteurs de risque du glaucome à pression normale et également des facteurs de risque d’évolution du glaucome.
- On constate également fréquemment des anomalies hémorhéologiques : anémie, hyper-viscosité sanguine et troubles du métabolisme des lipides.
- Le syndrome vaso-spastique périphérique (maladie de Raynaud) et central (migraines) sont également plus fréquemment rencontrés que dans la population générale. Mais la migraine ne semble pas être un facteur de mauvais pronostic.
- On constate également des anomalies de la microcirculation choroïdienne (avec atrophie péripapillaire visible au fond d’oeil) et rétinienne avec des spasmes vasculaires visibles en rétinographie et encore mieux identifiables en angiographie rétinienne à la fluorescéine. Les angio-OCT vont certainement nous apprendre beaucoup de choses dans les années à venir.
- Dans 5 à 7 % des glaucomes à pression normale graves, il est retrouvé un syndrome d’apnées du sommeil de type obstructif. Nous savons que cette maladie induit en outre un syndrome métabolique avec micro et macro angiopathie.
Mais les atteintes vasculaires de la tête du nerf optique ne donnent pas d’excavation papillaire sauf dans l’ischémie aiguë de la tête du nerf optique d’origine artéritique de la maladie de Horton. On peut donc difficilement expliquer cette différence d’aspect de la tête du nerf optique dans les autres pathologies vasculaires et le GPN. S’il y a un déterminisme vasculaire dans le glaucome à pression normale, il n’est pas univoque.
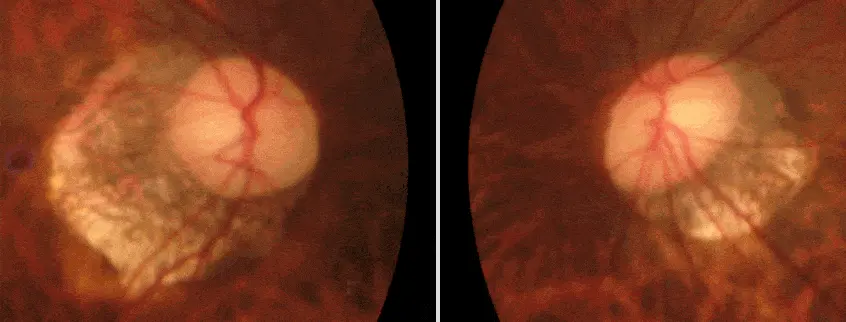
Un exemple caractéristique
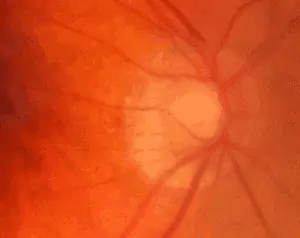
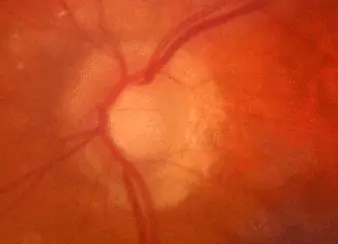
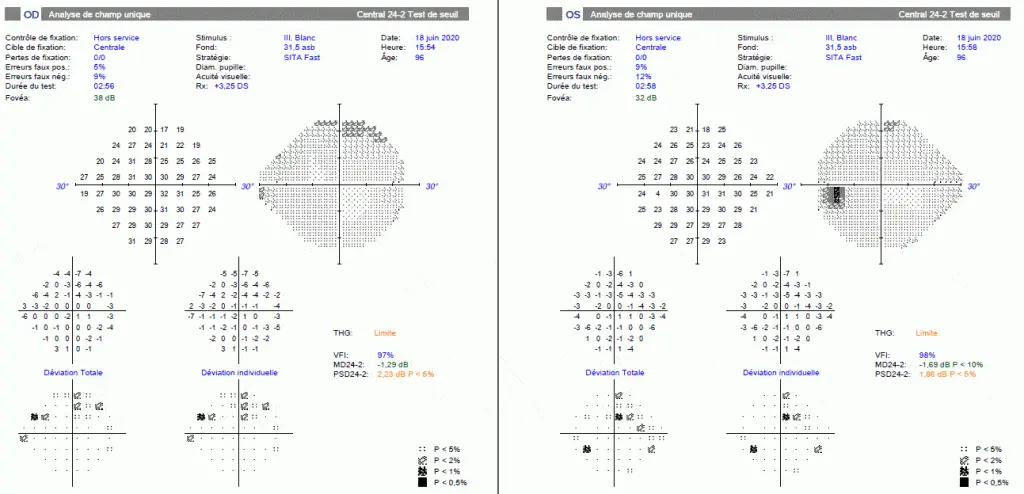
Patient de 94 ans présentant un lourd passé vasculaire d’origine athéromateuse, dont la tension oculaire est toujours restée basse entre 10 et 14 mmHg sans traitement, et qui présente au fond d’œil une atteinte du nerf optique très caractéristique avec rejet nasal des vaisseaux et profonde excavation. A noter une atrophie péripapillaire très importante d’origine ischémique. Le champ visuel et l’OCT n’ont jamais montré d’anomalies notables.

La théorie mécanique
Il y a de nombreuses années que les ophtalmologistes sont intrigués d’observer les mêmes modifications de type glaucomateux au niveau du nerf optique alors que la tension oculaire reste basse. Il a été évoqué depuis longtemps la possibilité d’une tension oculaire qui serait élevée mais qui n’aurait pas été appréciée correctement en raison notamment d’une pachymétrie cornéenne basse, et qui entraine des modifications mécaniques identiques au niveau de la lame criblée. Il a été évoqué également une fragilité particulière de la lame criblée, fine et fragile (cf infra : myopie forte et glaucomes évolués). En tout état de cause, c’est bien au niveau de la lame criblée (lamina cribosa) que tout se joue, mais pas de la même façon que dans le glaucome pressionnel (à tension oculaire élevée).
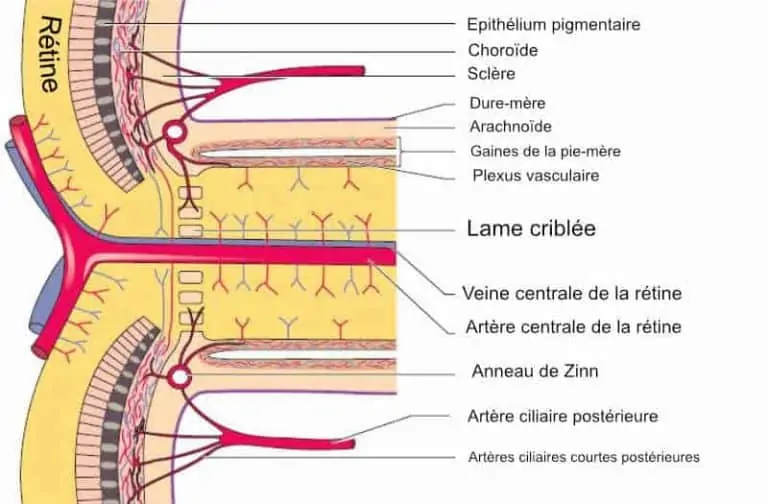
Coupe de la tête du nerf optique
La lamina cribosa n’est pas seulement soumise aux contraintes de la pression intra-oculaire. Sur cette hémi-coupe longitudinale de la tête du nerf optique, il existe des contraintes vasculaires exercées par les artères cérébrales, et des contraintes exercées par le liquide céphalo-rachidien (LCR) qui baigne l’espace sous-arachnoïdien, entre la pie-mère et la dure-mère, en rapport avec le LCR des espaces liquidiens intra-cérébraux.
La théorie de compartimentalisation du nerf optique
Le nerf optique est une émanation du cerveau, et à ce titre il est dépendant du flux du LCR qui lui permet d’éliminer les métabolites toxiques qui sont produits par l’activité neuronale. Lorsque les artères cérébrales perdent leur élasticité avec l’age, il existe une diminution de pulsatilité du flux de LCR et de l’élimination des déchets du liquide interstitiel cérébral. Il se produit une diminution du turn-over du LCR avec stase de LCR en périoptique. Ceci se traduit en IRM par une dilatation des espaces de Virchow-Robin au niveau du cerveau et d’une dilatation des gaines du nerf optique au niveau orbitaire. Inversement, un effet protecteur sur le glaucome peut être observé en cas de pression intracrânienne haute car le turnover du LCR serait alors augmenté.
La maladie d’Alzheimer est considérée comme étant consécutive à une différence entre la production et l’élimination des neurotoxines. Dans cette maladie, il existe 0 % de patients ayant une HTO (hypertension oculaire) alors que ce pourcentage est de 7% dans la population normale. Mais cependant il y a 25,9 % de GPAO chez les patients atteints de maladie d’Alzheimer alors que ce pourcentage n’est que de 5,2 dans la population générale. Tout se passe donc comme si le nerf optique était particulièrement sensible à l’hypertonie oculaire en raison de la stase LCR en rétro bulbaire.
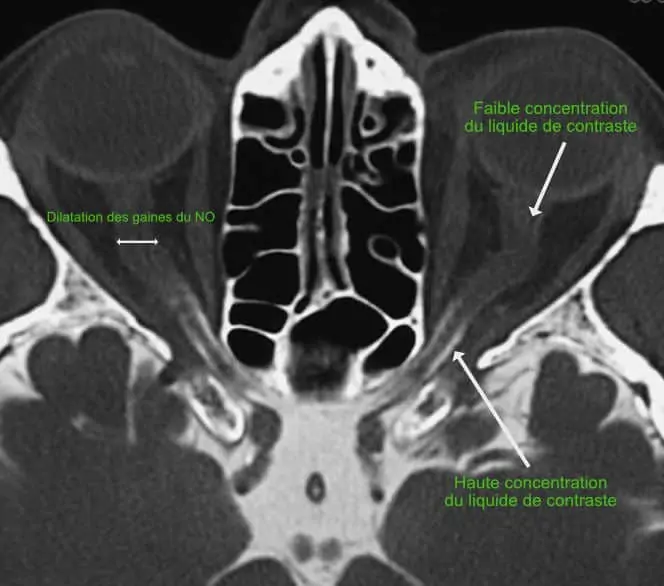
Lorsqu’on injecte un produit de contraste dans les espaces sous-arachnoïdiens et qu’on réalise un scanner, on peut visualiser le flux de LCR dans les gaines du nerf optique. Sur ce cliché, il existe une stagnation du LCR dans la portion rétrobulbaire du NO, et tout se passe comme si il existait un arrêt du flux de LCR avec constitution d’un compartiment séparé de moindre turn-over. Les axones au niveau de la lame criblée dégénèrent et disparaissent. On observe alors une excavation papillaire au FO.
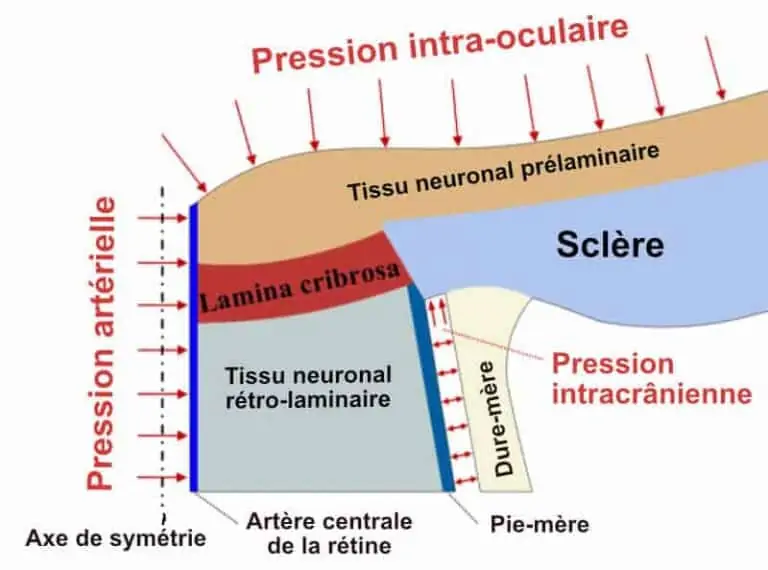
La théorie du gradient de pression translaminaire
Cette hypothèse tient compte de la pression du LCR s’exerçant sur la lamina cribosa : lorsque la pression intraoculaire est normale alors que la papille est excavée, c’est parce que la pression du liquide céphalorachidien est anormale que s’installe la souffrance du nerf optique. Ce qui compte c’est le gradient translaminaire, de part et d’autre de la lame criblée, induisant des contraintes de cisaillement et la dégénérescence rétrograde des neurones du NO. Cette théorie correspond à deux situations différentes :
- la pression du LCR est trop basse, traduisant une pression intracérébrale (PIC) faible que l’on peut mesurer par ponction lombaire. Cette situation se rencontre avec l’age, en cas d’hypotension artérielle, notamment diastolique, et chez le sujet de faible masse corporelle. La mesure de la PIC est de 9,5 mmHg en moyenne chez les patients ayant un GPN, elle est de 11,7 mmHg chez les patients ayant un GPAO et elle est de 12,9 mmHg dans la population normale. La pression translaminaire moyenne est donc de 12,5 mmHg dans le GPAO, de 6,6 mmHg dans le GPN et 4 mmHg en l’absence de glaucome. C’est le gradient de pression translaminaire qui est corrélé au déficit du champ visuel. Il est bien établi par de nombreuses études que le gradient de pression dans le GPN est consécutif à une pression basse du liquide céphalo-rachidien. La baisse de la pression intraoculaire permet donc de diminuer ce gradient de pression. La PIC est bien évaluée par l’espace sous arachnoïdien périoptique en IRM : il est significativement plus petit dans les GPN que dans les GPAO et que chez les sujets contrôles normaux.
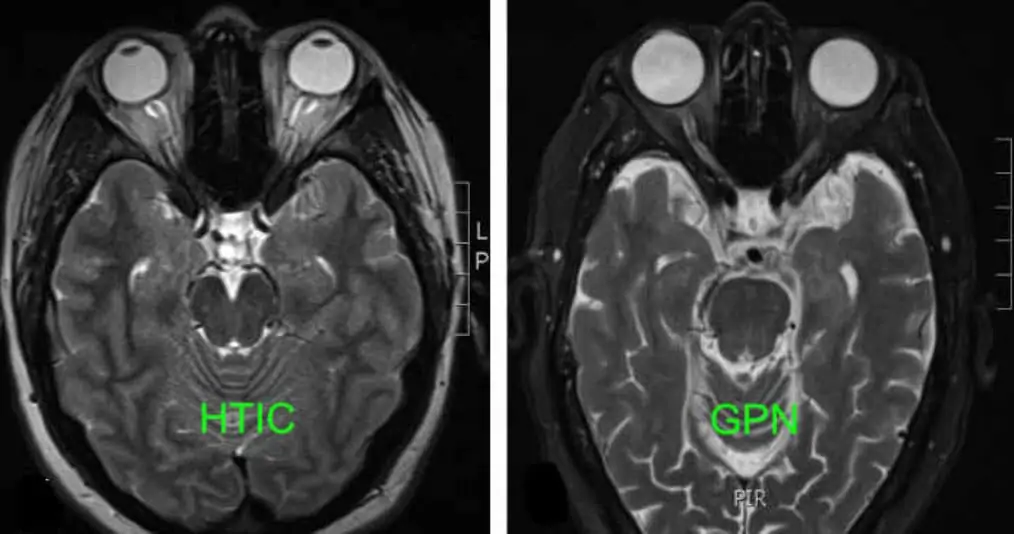
- la pression du LCR est trop haute, avec inversion du gradient de pression translaminaire, que l’on rencontre en cas d’hypertension intracrânienne chronique (HTIC). Une dilatation de la gaine des nerfs optiques est un signe d’HTIC lorsque les signes cliniques sont concordants : céphalées, acouphènes, vertiges, photophobie. Le patient est souvent photophobe, il peut avoir des fluctuations de la fonction visuelle, et il décrit souvent des signes visuels anormaux positifs ou négatifs (obscurcissement du champ visuel, troubles du champ visuel non visibles sur le relevé périmétrique, perception de phosphènes, de lumière anormale et parfois même authentiques hallucinations visuelles). La douleur rétro-bulbaire, les douleurs péri-orbitaires sont des douleurs rapportées liées à la dilatation de la gaine du nerf optique. Elles sont fréquentes et ne cèdent qu’aux diurétiques inhibiteurs de la synthèse du LCR. L’épreuve thérapeutique (après avoir éliminé une hypotension intracrânienne) au Diamox ou au Furosémide permet d’amender les signes cliniques et de restaurer partiellement le déficit fonctionnel du champ visuel.
.
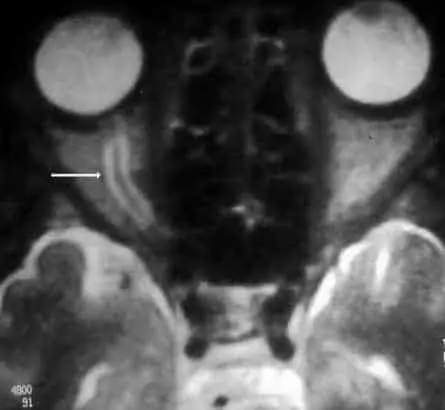
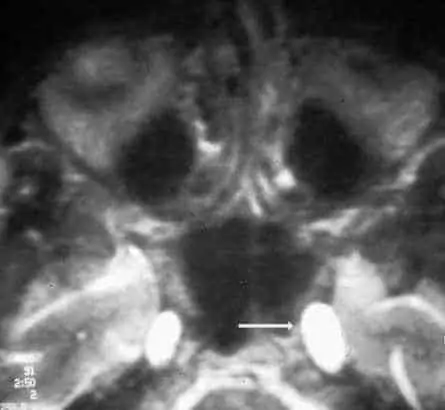
Le calibre du nerf optique orbitaire est augmenté (cliché de gauche) en cas d’HTIC, notamment dans sa portion distale juste rétrobulbaire (renflement terminal). Au contraire, ce calibre est diminué (cliché de droite) en cas d’hypotension du LCR avec un aspect de petit nerf optique.
Tous les clichés radiologiques présentés ici ont été réalisés à la Clinique Mutualiste de Pessac et nous voudrions remercier le Dr Pascal Kien qui en a assuré l’interpratation.
Quelques tableaux particuliers
L'hypertension intracrânienne chronique (HTIC)
La majorité des patients souffrant d’HTIC ne présentent aucune cause apparente pouvant expliquer leur affection, hormis des facteurs de risque comme le sexe féminin, l’obésité, les problèmes hormonaux et la prise de certains médicaments : minocycline, tétracycline, cimétidine, acide nalidixique, nitrofurantoine, indométacine, kétoprofen, isotretinoin, lithium, vitamine A (excès ou déficience), lévothyroxine, triméthoprim-sulfaméthoxazole, corticostéroïdes (sevrage), tamoxifen, hormone de croissance, … et la liste n’est pas close. De nombreuses pathologies ont également été associées à l’HTIC, sans qu’un un lien de causalité puisse nécessairement être démontré : lupus érythémateux systémique, hypoparathyroïdie, maladie d’Addison, sarcoïdose, hyperthyroïdie, anémie, … la liste là aussi s’allonge au fur et à mesure que les techniques d’investigation médicale se modernisent, conduisant à de nombreuses observations cliniques. Parmi celles-ci, trois tableaux cliniques possèdent une individualité remarquable:
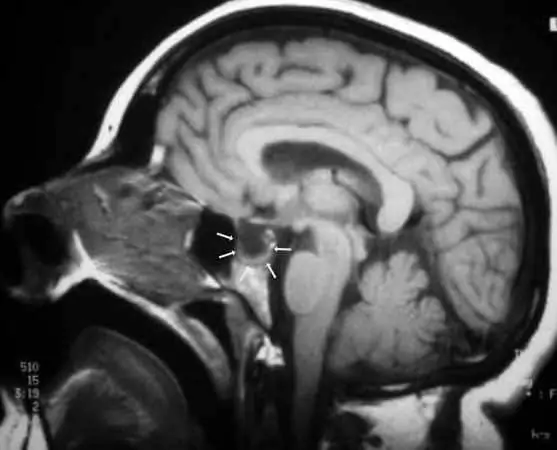
1 – Le syndrome de la selle turcique vide : de découverte radiologique dans le bilan d’un syndrome clinique d’HTIC, elle est un symptôme radiologique d’augmentation de la pression du LCR mais bien entendu un bilan hormonal complet doit être mis en oeuvre pour determiner si une pathologie hypophysaire explique les images radiologiques.
2- La myopie forte et les glaucomes évolués : Le gradient de pression translaminaire dépend de la pression intraoculaire, de la pression intracrânienne, mais également de l’épaisseur de la lame criblée. Plus la lame criblée est fine plus le gradient de pression induit des contraintes de cisaillement au niveau des axones qui traversent la lame criblée. L’épaisseur de la lame criblée diminue avec la progression du glaucome. Ce phénomène explique que dans certains glaucomes la neuropathie optique évolue alors que la pression intraoculaire est normalisée. Chez le myope fort avec une longueur axiale supérieure à 26 mm, plus le disque est grand plus la lame criblée est fine et plus le risque de glaucome semble augmenter. (Voir schéma plus loin).
3- Le syndrome d’apnées du sommeil : Le syndrome d’apnées du sommeil (SAS) est fréquemment associé au GPN, sans qu’un mécanisme unique ne puisse être certifié. Mais comme dans la selle turcique vide radiologique, l’HTIC est univoque et explique les anomalies visuelles. Dans le SAS, l’hypertension intracrânienne est nocturne. À chaque apnée, il existe une montée de la PIC qui se traduit selon la loi de LAPLACE par une pression exercée à la partie distale du nerf optique en rétro bulbaire (d’ailleurs l’association œdème papillaire et SAS est classique). Plusieurs observations témoignent d’une augmentation de la PIC dans le syndrome d’apnée du sommeil : œdème papillaire, occlusion de la veine centrale de la rétine le matin au réveil (pendant toute la nuit la PIC augmentée favorise le défaut du drainage veineux) et choriorétinopathie séreuse centrale (CRSC). Dans la CRSC il a été incriminée, avec l’augmentation de la PIC, une augmentation du volume choroïdien et parfois même supraciliaire avec un angle irido-cornéen étroit (syndrome du joueur d’instrument à vent) . Seuls 5 % des patients ayant un syndrome d’apnée du sommeil possèdent un GPN mais 50% des GPN auraient un syndrome d’apnée du sommeil. Dans notre expérience, la prise en charge d’une augmentation de la PIC s’accompagne d’une réversibilité plus ou moins importante des déficits du champ visuel.
Selle turcique vide
La selle turcique vide est une arachnoidocèle intrasellaire avec absence totale ou partielle du contenu sellaire à l’IRM ou au scanner. On observe que le parenchyme hypophysaire est tassé au fond de la selle turcique. Elle peut être primitive par anomalies congénitales du diaphragme sellaire, ou secondaire à une pathologie locale (thyroïde, tumeur du chiasma). La proximité des voies optiques antérieures qui sont juste au-dessus du diaphragme sellaire pose un problème étiopathogénique très important en face de problèmes visuels mimant un GPN avec excavation papillaire. Des mécanismes vasculaires compressifs ont pu être évoqués pour expliquer les anomalies retrouvées au CV.
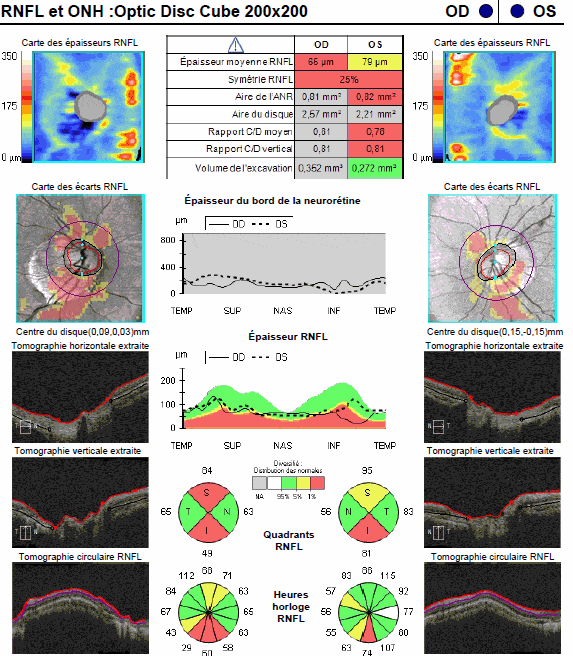
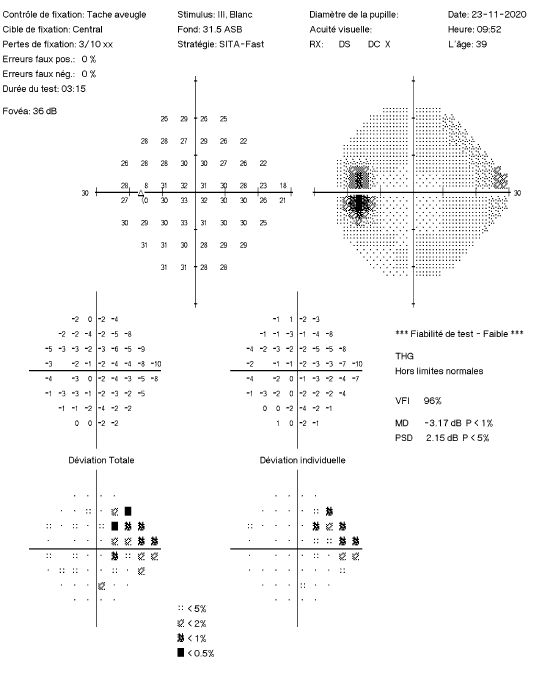
L’OCT montre un effondrement de l’épaisseur du bord de la neuro-rétine et du RNFL en temporal, difficile à interpréter en raison de l’importance de l’atrophie péripapillaire. Mais le champ visuel montre un scotome temporal supérieur à doite, indépendant de l’atrophie, signant le diagnostic de GPN.
Pour conclure ce chapitre complexe du glaucome à pression normale
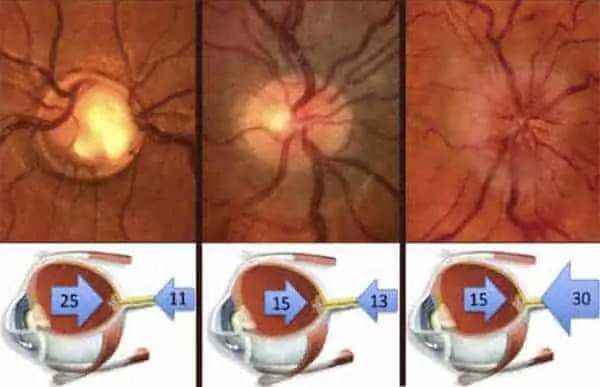
Il n’existe pas de parallélisme anatomoclinique parfait dans beaucoup de situations cliniques mimant un glaucome pressionnel. On pourrait résumer grossièrement la situation par un schéma qui vaut ce qu’il vaut mais qui a le mérite d’être clair.
En l’absence de glaucome, la pression intra-oculaire (PIO) et la pression du LCR en péri-optique s’équilibrent (au milieu). Lorsque la PIO est très élevée ou que la pression du liquide céphalo-rachidien est très élevée (à droite), il apparaît un œdème papillaire consécutif au gonflement des axones au niveau de la lame criblée par arrêt des transports axoplasmiques orthograde et rétrograde. Lorsque la PIO est modérément élevée comme dans le glaucome (à gauche) il existe une perte axonale orthograde lentement progressive qui se traduit par une excavation papillaire. Lorsqu’il existe une inversion du gradient de pression de part et d’autre de la lame criblée, il apparaît également une excavation papillaire mais par un mécanisme rétrograde.
Le glaucome à pression normale est un groupe hétérogène de patients
- Chez le myope le déterminisme principal est la finesse de la lame criblée.
- Chez la personne d’un grand âge, le déterminisme principal est la baisse de la pression du liquide céphalo-rachidien
- Dans la maladie d’Alzheimer, le glaucome à pression normale serait lié à une accumulation de neuro-toxines avec un défaut du turnover du LCR. Mais l’IRM peut montrer un aspect de « petit nerf optique » lorsque la pression du LCR est faible en arrière de la tête du nerf optique et que les gaines du NO sont collabées autour de lui, ou au contraire un aspect dilaté du nerf optique lorsque la stase du LCR est importante.
- Dans le syndrome d’apnée du sommeil, au début du processus pathologique, avant que ne se surajoute un déterminisme vasculaire, l’inversion du gradient de pression mime un glaucome à pression normale dont la caractéristique est l’amélioration du cours évolutif par les traitements permettant de diminuer les poussées de la pression intracrânienne. Mais selon l’importance et le sens du gradient de pression translaminaire, on peut observer un GPN, un glaucome pressionnel classique, ou une poussée aiguë de la pression intracrânienne avec oedème papillaire.